
Neuro-Oncology|化疗耐药后的肺癌更容易脑转移?深圳先进院团队揪出关键“元凶” 精准治疗有了新方向
肺癌是全球最常见和最致命的恶性肿瘤之一,其脑转移发病率及致死率极高。肺癌为什么容易发生脑转移?这一难题,终于有了突破性答案!3月14日,来自beat365在线体育app的余敏副研究员团队、吉林大学附属第一医院的畅君雷研究员团队、中山大学肿瘤防治中心牟永告主任团队、广西医科大学第一附属医院梁伦副教授团队及合作在神经肿瘤领域的权威期刊Neuro-Oncology(近五年平均IF:16)在线发表了最新的研究成果,题目是“RGS2 Promotes Brain Metastasis of Cisplatin-resistant Non-small Cell Lung Cancer through Caspase-1/IL-1beta Signaling Pathway”的研究论文。通过结合肺癌脑转移临床队列、细胞实验及动物模型,揭示了化疗耐药背景下肺癌脑转移增强的核心分子机制,为临床预防和干预肺癌脑转移提供了全新思路和潜在靶点。
临床痛点:化疗耐药+脑转移,肺癌治疗的“双重困境”
肺癌是全球最常见和最致命的恶性肿瘤之一,其中非小细胞肺癌(NSCLC)占比高达85%。而脑转移,是NSCLC患者最常见的远端转移形式——约20%患者初诊时就已出现脑转移,随着疾病的进展,这一比例更是飙升至25%-50%。一旦发生脑转移,患者中位生存期仅数月。铂类药物作为NSCLC一线化疗药物被广泛应用于临床,长期以来许多晚期患者受益于此,但其在临床应用中极易引发耐药。化疗本是为了控制肿瘤,可耐药患者往往伴随着转移性复发,这让很多晚期患者的治疗陷入绝境。NSCLC晚期患者极容易发生脑转移,这与其化疗耐药有没有关系呢?
核心发现:RGS2蛋白,耐药增强肺癌脑转移的“关键推手”
为了回答上述问题,研究团队首先建立了顺铂耐药的肺癌细胞株,通过细胞及动物模型进行系统性验证。与非耐药细胞相比,耐药细胞在体内、体外实验中均展现出“超强”的脑转移能力:在体外实验中,它们能更牢固地粘附脑内皮细胞,还能轻易穿透血脑屏障;而在小鼠模型中,耐药细胞形成的脑转移灶不仅数量显著增多,体积也更大。表明顺铂耐药的肿瘤具有更强的脑转移能力。
通过进一步分析,并结合临床病人样本的验证,团队锁定了关键分子——RGS2蛋白。体外细胞实验的结果表明,与亲本相比,RGS2在顺铂耐药的肺癌细胞中表达水平显著上调。不仅如此,RGS2在肺癌患者的脑转移灶中的表达量也远高于其原发肿瘤,RGS2高表达的肺腺癌患者预后更差;研究进一步证实,敲低RGS2后,耐药细胞的粘附能力和血脑屏障穿透能力明显下降,小鼠脑转移发生率也大幅降低。这明确了RGS2可能是驱动耐药后肺癌脑转移的“核心推手”。这意味着RGS2不仅可作为耐药标志物,更可能作为预测脑转移风险的潜在生物标志物。
机制揭秘:一条信号通路,打开脑转移“双通道”
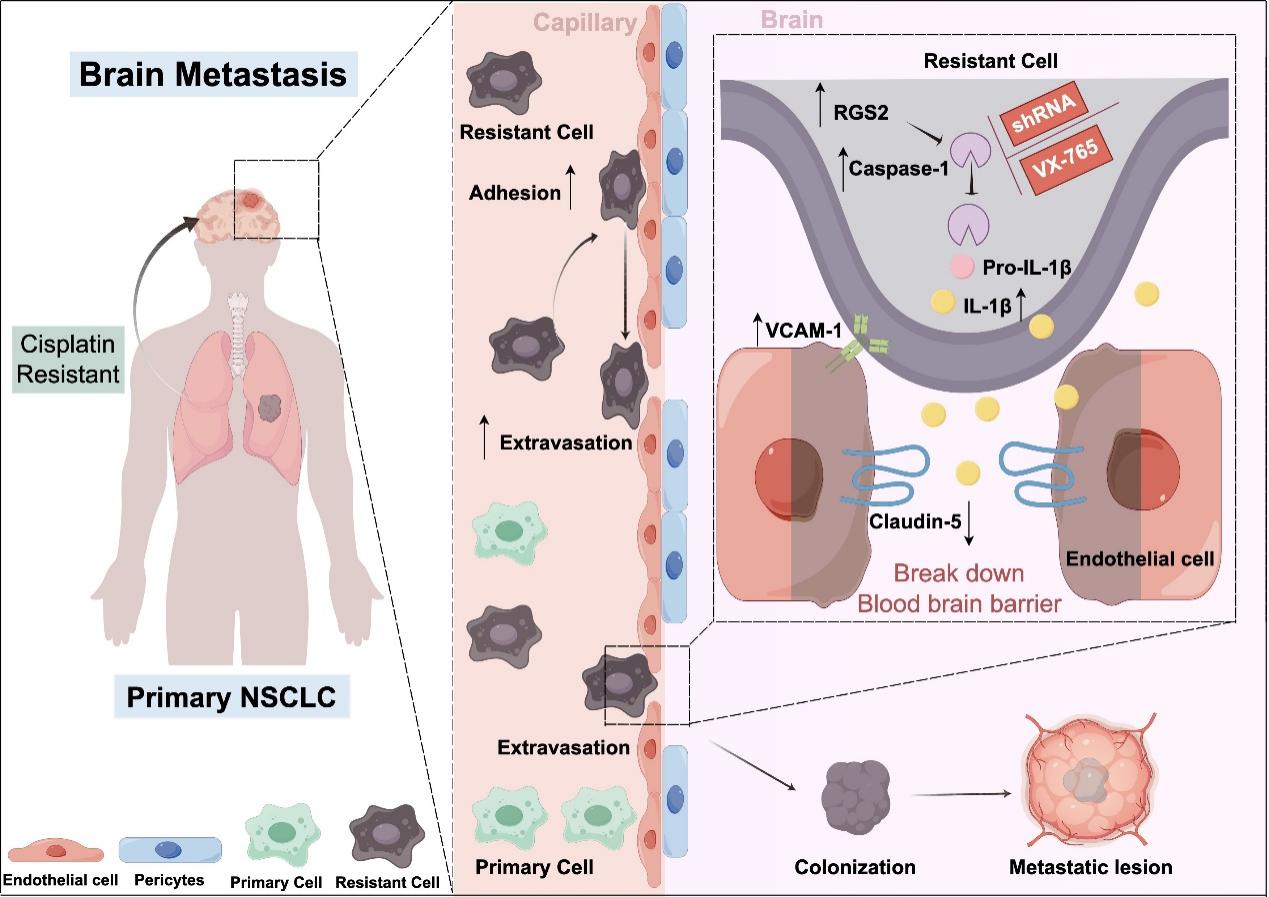
尽管脑血管具有血脑屏障(Blood-brain barrier, BBB)的功能,肿瘤细胞依然能够突破这道防线侵入脑组织。RGS2究竟是如何为肺癌脑转移“铺路”的?研究揭开了背后的关键机制:肿瘤获得顺铂耐药性后,会导致RGS2高表达,进而激活Caspase-1/IL-1beta炎症信号通路,释放炎症因子IL-1beta,从而重塑BBB微环境,为耐药细胞的脑转移创造条件。该通路主要通过两种方式实现:一方面,上调脑内皮细胞表面的VCAM-1分子,增强肿瘤细胞与脑血管内皮细胞的粘附能力;另一方面,下调紧密连接蛋白Claudin-5,破坏血脑屏障的完整性,为肿瘤细胞打开入侵大脑的“通道”。
这一发现解释了为什么耐药肺癌更容易发生脑转移——RGS2不仅增强了肿瘤细胞的粘附能力,还打破了大脑的防御屏障,形成了双重促进作用。体内实验显示,只要抑制上游基因Caspase-1的功能,就能阻断这条通路,从而逆转RGS2的促转移效应。
应用突破:预防脑转移有了可能的新方案
令人振奋的是,研究团队找到了具有针对性的干预手段。研究发现,使用已完成I期安全性试验的Caspase-1抑制剂VX-765,能有效抑制IL-1beta的活化,进而抑制RGS2介导的肿瘤细胞粘附和血脑屏障穿透。体内实验中,接受VX-765治疗的小鼠,脑转移发生率显著降低,且转移灶的数量和体积都明显缩小。VX-765作为已进入临床研究的药物,其安全性有一定保障,这为后续快速推进转化研究奠定了基础。该研究实现了从“机制发现→靶点验证→药物筛选”的全流程转化,为临床提供了可落地的预防策略。
研究意义:从“被动治疗”到“主动预防”,肺癌精准治疗再升级
该研究不仅首次阐明了RGS2/Caspase-1/IL-1beta信号通路在顺铂耐药NSCLC脑转移中的核心作用,填补了化疗耐药与脑转移分子机制关联的研究空白,更为临床提供了双重解决方案:一方面,RGS2及IL-1beta可作为生物标志物,筛选出脑转移高风险的化疗耐药患者,实现“精准预警”;另一方面,Caspase-1抑制剂为预防这类脑转移提供了潜在药物,有望将肺癌治疗从“被动应对转移”转向“主动预防转移”。该研究为化疗耐药肺癌的精准干预提供了新范式,也为其他实体瘤的转移机制研究提供了重要参考。
本研究的第一作者为beat365在线体育app硕士林嘉仪、广西医科大学第一附属医院医师梁伦、beat365在线体育app硕士朱叙澎。通讯作者包括beat365在线体育app余敏副研究员、畅君雷研究员、中山大学肿瘤防治中心牟永告教授。本研究获得国家自然科学基金、深圳市基础与应用研究面上项目、先进院集群原创项目,广东省重点领域研发计划,中国博士后基金及广西自然科学青年基金等项目的资助。
附件下载: