
Experimental & Molecular Medicine|深圳先进院揭示代谢功能障碍相关脂肪性肝病的“糖异生-表观遗传修饰”交流调控新机制
代谢功能障碍相关脂肪性肝病是全球范围内最常见的慢性肝病之一,可进一步进展为肝硬化甚至肝细胞癌。衰老、久坐生活方式及营养过剩等因素显著增加功能障碍相关脂肪性肝病/肝炎(MASLD/MASH)的发生风险。
5月8日,beat365在线体育app(以下简称“深圳先进院”)管敏研究团队在国际权威期刊Experimental & Molecular Medicine杂志发表最新研究"Hepatocyte estrogen-related receptor α modulates a gluconeogenic–epigenetic crosstalk counteracting MASLD/MASH progression"。该研究解析了肝细胞中代谢介导表观遗传修饰在MASLD/MASH进展中的关键作用,揭示了肝脏雌激素相关受体α(ESRRA)通过调控糖异生影响组蛋白乳酰化修饰,减轻MASLD/MASH病理进程的分子机制。
研究人员首先在衰老、高脂高胆固醇饮食及化学药物等多种风险因素诱导的MASLD/MASH小鼠模型中观察到,肝脏ESRRA表达水平明显下降,同时伴有乳酸和组蛋白乳酰化(H3K18la)水平显著升高。在老年小鼠中,这种代谢与表观遗传的失衡可被长期运动缓解,而在肝细胞特异性敲除ESRRA时则进一步加重,提示ESRRA在介导运动代谢与表观遗传调控之间发挥关键桥梁作用。
机制研究表明,运动诱导的ESRRA与其经典共激活因子PPARGC1A协同作用,通过转录调控乳酸脱氢酶B(LDHB)和葡萄糖-6-磷酸酶(G6PC1),增强乳酸-葡萄糖代谢转变,将乳酸从“乳酰供体”角色转变为“糖异生前体”,减少MASH相关基因启动子区域H3K18la的异常富集。
体内实验证实,肝脏特异表达递送系统AAV8-TBG长效表达ESRRA基因,可显著缓解小鼠MASH模型的肝脏病理,同时纠正异常H3K18la积累及其驱动的病理基因表达谱。相反,ESRRA缺失则加重疾病表型。
该研究阐明了靶向肝脏ESRRA调节乳酸代谢、重塑组蛋白乳酰化水平的“糖异生代谢-表观遗传”交流调控轴。该发现有助于进一步了解不同疾病风险因素驱动的MASLD/MASH病理机制,为开发MASLD/MASH治疗策略提供了新的理论依据和潜在靶点。
深圳先进院管敏研究员为本论文通讯作者。深圳先进院科研助理高军及广东医科大学杨萌博士(先进院毕业博士生)为第一作者。华南师范大学体育科学与运动学院院长段锐教授及中科院昆明植物研究所耿长安研究员为本研究提供了重要支持。
该研究获得国家重点研发计划、国家自然科学基金、深圳市医学研究基金、深圳市科技计划、中国科学院“西部之光”跨学科团队项目、植物化学与天然药物国家重点实验室开放课题等项目的资助。

文章上线截图
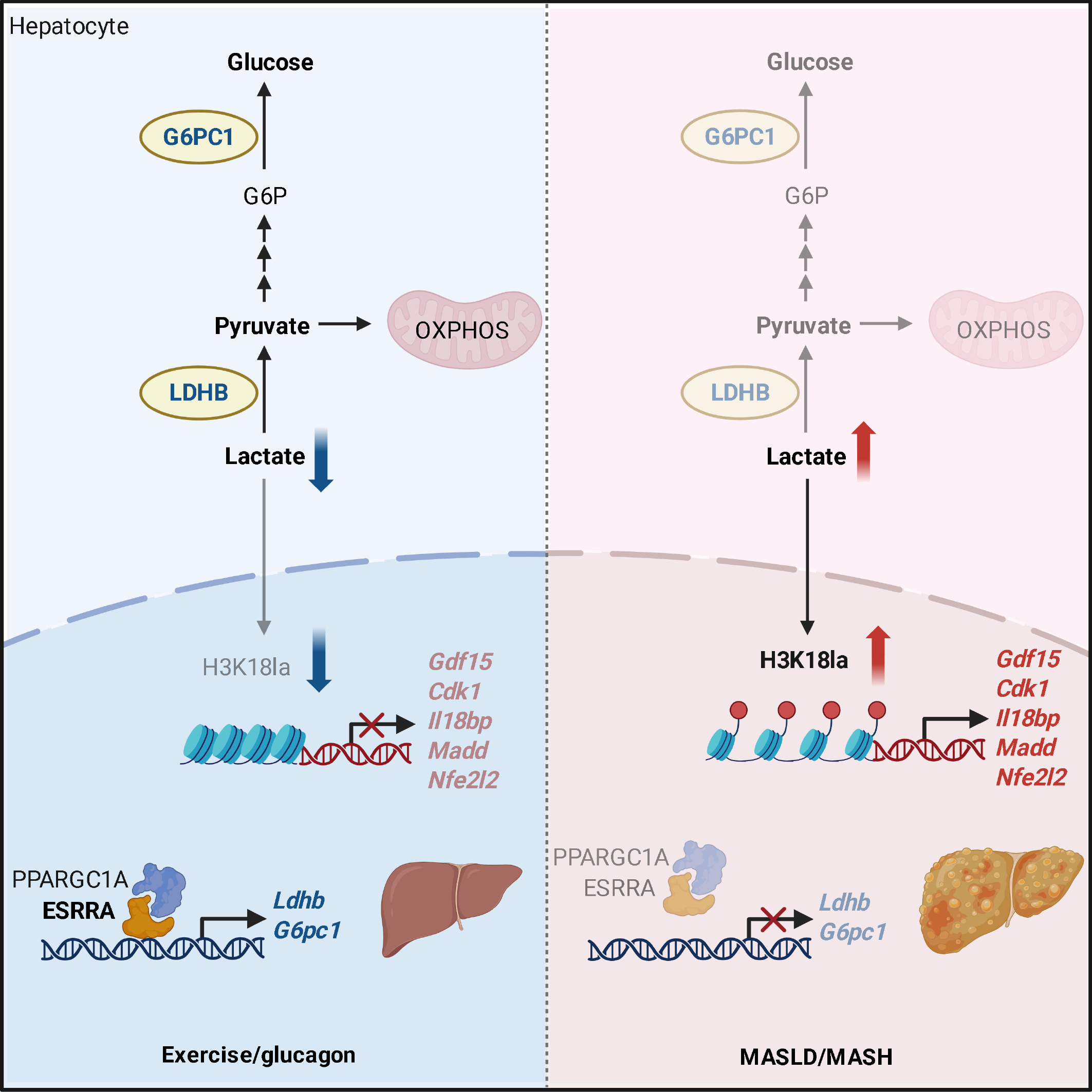
肝脏ESRRA调控糖异生-表观遗传修饰干预MASLD/MASH机制示意图
附件下载: