
Cell Host & Microbe | 深圳先进院发现肠道噬菌体隐藏“免疫开关”——全新抗CRISPR蛋白家族
在我们每个人的肠道里,数万亿细菌与它们的“天敌”——噬菌体,正上演着一场持续亿万年的“军备竞赛”。CRISPR-Cas系统被誉为细菌的“免疫系统”,能精准识别并切割入侵噬菌体的DNA。然而,噬菌体为了生存,进化出了“抗CRISPR蛋白”(Acr),能够“蒙蔽”或“关闭”细菌的CRISPR防御。这一攻防机制不仅是微生物世界的“军备竞赛”,也为我们提供了调控基因编辑工具的天然“开关”。但迄今为止,人类肠道作为微生物最密集、互作最复杂的生态系统之一,其噬菌体所携带的Acr却鲜少被系统研究。
近日,beat365在线体育app定量合成生物学全国重点实验室、合成微生物组学研究中心马迎飞团队成功从人类肠道噬菌体中,发现了一大批能够抑制II型CRISPR系统的Acr,并揭示了一类全新的、结构高度相似却机制多样的抗CRISPR蛋白家族——GutAcraca。相关研究成果发表于国际权威期刊Cell Host & Microbe,为理解肠道微生物互作机制以及开发新型基因编辑调控工具提供了新的视角。
II型CRISPR系统在肠道中占主导地位
在深入挖掘肠道噬菌体的抗CRISPR蛋白之前,研究团队首先对肠道细菌的“防御武器库”进行了全面普查。通过对人类肠道菌数据库(UHGG)中近28.7万个细菌基因组的系统分析,一个此前被低估的现象浮出水面:在人类肠道中,II型CRISPR系统(以Cas9蛋白为核心)占据了绝对的主导地位,占所有已识别CRISPR系统的47%。这一比例远超传统认知中在其它环境中更为普遍存在的I型系统。研究还发现,其中相当一部分的CRISPR RNA(crRNA)能够精准匹配到肠道病毒组的噬菌体序列。这一发现为后续研究提供了坚实的理论基础:既然肠道细菌普遍装备了强大的II型CRISPR免疫系统,那么作为其宿主的噬菌体,必然进化出了同样多样且高效的抑制策略来突破这道防线。
肠道噬菌体是Acr的“宝库”
基于上述发现,研究团队开发了一套整合大规模生物信息学分析与高通量功能筛选的实验体系,旨在系统性地“捕获”肠道噬菌体编码的Acr。他们首先利用CRISPR间隔区与病毒序列的匹配信息,锁定了那些正与细菌进行激烈攻防的噬菌体。随后,结合“guilt by association”等策略,从33,242个肠道病毒基因组中筛选出13,493个候选基因。
为了高效验证这些海量候选基因的功能,团队构建了包含3,411个基因的高通量文库,并将其逐一导入携带六种不同II型Cas9(SpyCas9, SaCas9, St1Cas9, St3Cas9, FnCas9, NmCas9)的大肠杆菌报告菌株中进行功能筛选。通过多轮竞争性培养和深度测序,最终鉴定出651个能够帮助细菌在CRISPR免疫压力下存活的阳性Acr候选蛋白。研究团队从中随机选取了36个代表性候选者,通过噬菌斑形成实验,证实了它们确实能保护噬菌体免受CRISPR系统的攻击,抑制活性得到充分验证(图2)。这一结果强有力地证明,人类肠道是此前未被充分探索的Acr蛋白天然“宝库”,其多样性远超想象。
结构相似但功能各异的GutAcraca家族
在对这651个阳性Acr进行深入分析时,一个引人注目的现象出现了。通过AlphaFold2结构预测和TM-score结构相似性比对,研究团队发现一个由213个成员组成的巨大蛋白簇,这些蛋白尽管在氨基酸序列上差异巨大,却惊人地折叠出高度相似的三维结构(图3)。
这一发现挑战了领域内关于Acr蛋白“极端多样”的固有认知。研究人员将这个结构汇聚的蛋白家族命名为GutAcraca。通过对其中10个代表性成员的深入研究发现,它们不仅能够抑制多种Cas9同源物,展现出广泛的抑制谱,而且具备“双重功能”:既能像“断路器”一样抑制CRISPR系统,又能作为转录调控因子,与其自身的启动子结合,实现精准的自我表达调控(图3)。这种精巧的调控机制可能有助于噬菌体在整合到细菌基因组后,避免因过度表达Acr而造成不必要的代谢负担或毒性,体现了噬菌体对肠道生态的精细适应。
GutAcraca家族广泛存在于肠道微生物群落中
GutAcraca家族并非孤立存在。为深入理解其生态学意义,研究团队进一步将分析拓展至更广泛的肠道微生物群落。利用Foldseek结构搜索工具,他们发现GutAcraca的结构类似物广泛分布于高达26%的肠道微生物物种中,主要存在于溶原性噬菌体基因组上,遍及厚壁菌门、变形菌门、放线菌门等主要细菌类群。尤为值得注意的是,超过82%携带GutAcraca基因的噬菌体被预测为“温和噬菌体”,这类噬菌体常将自身DNA整合进细菌基因组形成原噬菌体,与宿主长期共存(图4)。这一发现提示,GutAcraca可能在噬菌体进入溶原状态时发挥关键作用:通过抑制细菌CRISPR系统的活性,保护自身DNA免遭宿主“自我免疫”攻击,从而成为温和噬菌体在复杂肠道环境中实现稳定存活与长期演化的重要适应策略。
新发现的抗CRISPR蛋白除具备上述功能特征外,还展现出若干独特的优势,为其应用奠定了坚实基础。首先,GutAcraca家族中超过72%的成员小于80个氨基酸。受此启发,团队设计出仅含28个氨基酸的超短肽段仍具抑制活性,为目前已知最小的抗CRISPR元件;其次,AcrIIB-1则是对FnCas9抑制活性最强的Acr(图5)。这些特征使其可作为基因编辑的“精准开关”,实现对CRISPR系统的按需调控,从而有效降低脱靶效应、提升基因治疗安全性。
肠道噬菌体不仅是细菌的捕食者,更是自然界进化的“创新工厂”。这项研究揭示了肠道噬菌体在长期进化中形成的“智慧”,也为人类利用这些天然分子调控工程细胞、构建合成细胞提供了全新思路。未来,随着更多功能性Acr蛋白的发现和应用,我们有望在基因治疗、合成生物学、肠道菌群调控等领域迎来新一轮突破。
beat365在线体育app助理研究员袁盛建、博士生朱衡及已出站博士后于梦浩为该论文共同第一作者。beat365在线体育app定量合成生物学全国重点实验室、微生物组学研究中心马迎飞研究员为该论文通讯作者。联培博士生贾汇真、研究实习员彭仕文为参与作者,对本项工作做出重要贡献。本项工作得到了国家重点研发计划、国家自然科学基金、深圳医学科学院、深圳合成生物学创新研究院等项目的大力支持。

文章上线截图
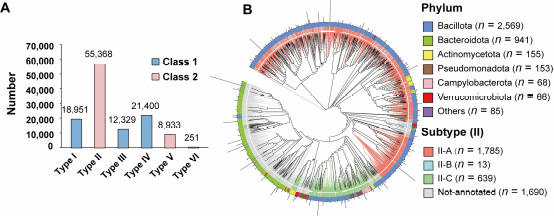
图1. CRISRP系统在肠道菌中的分布
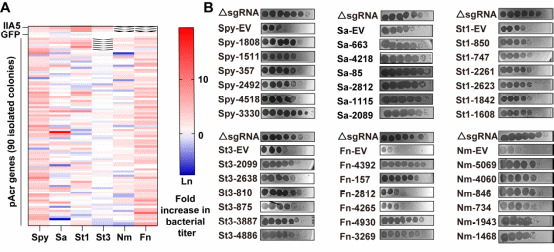
图2. 肠道噬菌体Acr的高通量挖掘和功能鉴定
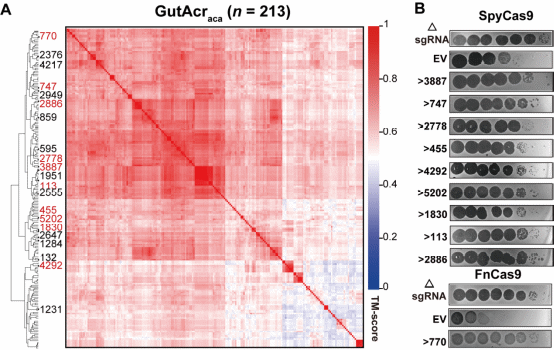
图3. 肠道噬菌体结构相似的GutAcraca家族功能鉴定
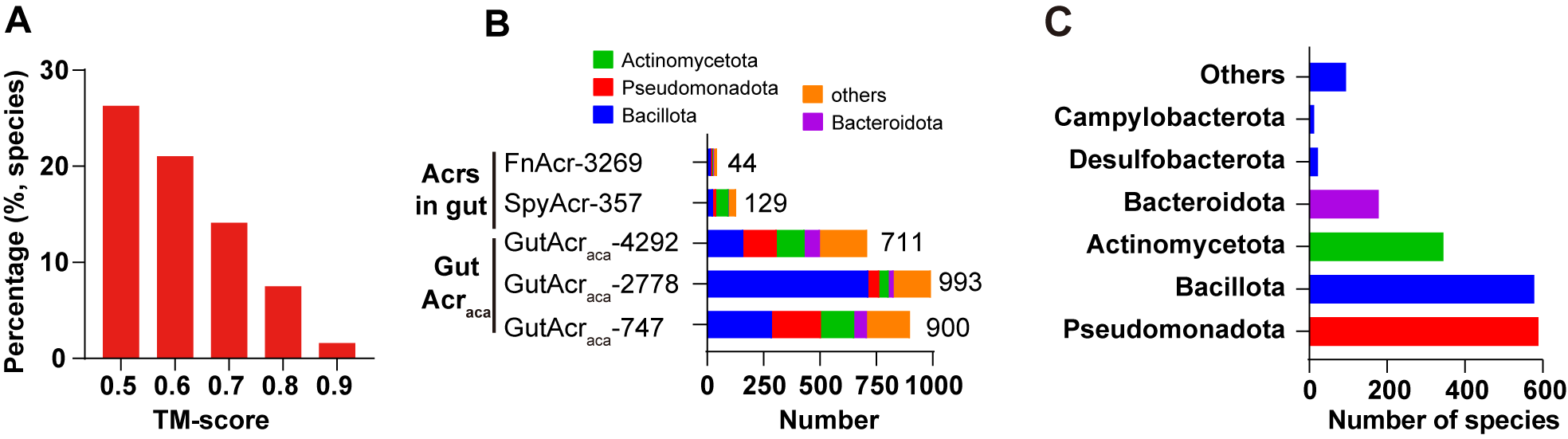
图4. GutAcraca家族在肠道菌群中的分布
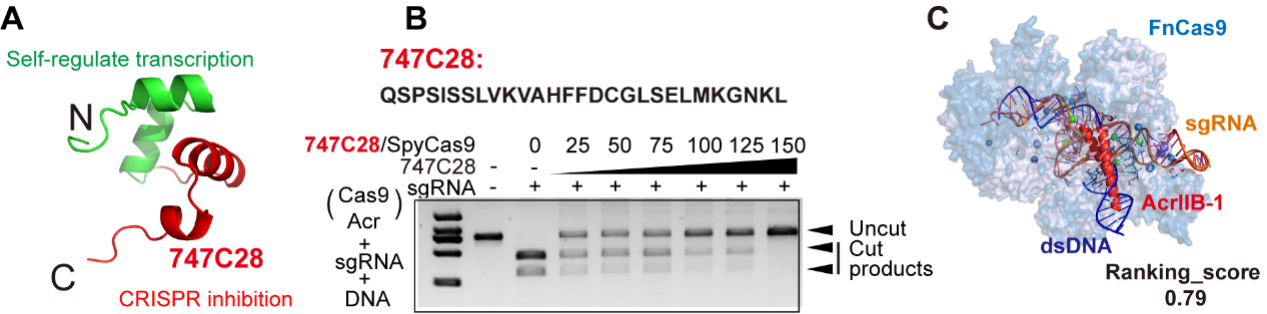
图5. 合成最小功能性Acr
附件下载: