
Neuron丨揭示骨源性激素—骨钙素作用经典奖赏中枢VTA启动逃跑反应
本能恐惧反应,是物种进化中形成的核心生存策略。这种对潜在天敌的快速应对机制,对于保障个体生存与物种延续至关重要。这一行为的调控机制不仅涉及中枢环路,也关乎中枢与外周信号的复杂相互调控机制(Tseng YT. et. al. Nature Reviews Neuroscience,2023),其功能异常往往与多种精神疾病密切相关,包括焦虑症、抑郁症和创伤后应激障碍等。因此,深入解析本能恐惧行为的脑体互作机制,不仅能揭示跨器官的功能协同调控物种生存行为的生物学本质,更为神经系统与其他器官共病的临床干预提供全新思路,还有望为生物启发的具身智能体开发提供新的洞见。
王立平研究员团队长期致力于本能行为的神经环路解析,以及中枢外周互作对机体稳态的调控机制和转化研究。团队通过神经环路示踪、光/药物遗传学、电生理、3D精细行为学、多组学等交叉前沿方法,围绕本能行为神经环路基础以及脑体互作调控机体稳态的机制这一核心科学问题,取得了一系列系统的、原创性研究成果,累计发表高水平学术论文130余篇,包括Neuron (7篇)、Nature Communications(6篇)等,并受邀在Nature Reviews Neuroscience、Neuron 等撰写综述论文。
2月11日,beat365在线体育app脑认知与脑疾病研究所/深港脑科学创新研究院、深圳理工大学王立平研究员、刘雪梅副研究员、李翔研究员、谭力铭研究员团队通力合作,在Neuron杂志上在线发表题为“A bone-derived hormone permits rapid visual escape via GPR37 receptor in a subpopulation of VTA GABAergic neurons”的研究论文,该研究首次揭示:骨骼释放的激素骨钙素(Osteocalcin, OCN)能够激活大脑腹侧被盖区(VTA)内共释放GABA与谷氨酸的神经元中表达的GPR37受体,通过cAMP-THIK-1这一非经典信号通路迅速增强此类神经元的兴奋性,进而驱动在急性天敌应激的快速逃跑反应。
模拟捕食者逼近的“视觉阴影刺激”(Looming)是研究本能恐惧反应的经典范式。王立平研究员团队于2015年在国际上率先证明了上丘到丘脑枕核到杏仁核的皮层下通路的结构的存在并处理视觉本能恐惧的新功能,回答了神经科学领域长达数十年的争议问题,文章至今被引用411次(Wei PF et al., Nature Communications, 2015);随后,进一步揭示了传统奖赏中枢——腹侧被盖区(VTA) 的特定GABA能神经元,是驱动快速逃跑行为的关键中继站,文章至今被引用达206次(Zhou Z & Liu XM et al., Neuron, 2019)。团队最新研究发现,急性天敌应激的恐惧反应存在个体差异,在恐惧高敏感个体中,这群VTA神经元会持续接收来自上丘的输入并输出到恐惧中枢杏仁核,维持一种持续的警觉状态(Liu XM et al., Neuron, 2025)。
然而,一个核心的基础性问题依然存在:机体中何种来自外周器官的信号能预先调控这些VTA的特定类型神经元功能状态,使其维持在高度警觉的"预备状态"(Permissive state),从而保障天敌来临时的快速逃跑反应? 这一关键核心问题的回答,在很大程度上将帮助我们深刻理解机体整体层次上器官间信息传递如何调控个体生存能力的底层科学逻辑。
在应激反应中,经典的外周激素如皮质酮、肾上腺素与等虽扮演关键角色,但传统研究往往聚焦于中枢神经机制,或关注这些激素对心率、血压等外周指标的快速影响,急性应激下尤其是机体面对生死攸关的天敌应激下,外周其他器官的调控信号如何重塑“体-脑”联动机制缺乏系统阐释。
近年来,骨骼作为内分泌器官的作用逐渐被重视。从进化角度看,骨骼不仅保护大脑,其与神经系统的协同进化也帮助生物应对环境挑战——例如中国科学院水生所何舜平、王文教授研究团队证明脊椎动物在从水生向陆地过渡的宏大演化历程中,与应激、焦虑相关的基因发生了显著变化。这表明,“登陆”这一重大环境剧变,可能在遗传层面筛选并强化了更具警觉性的个体,以应对陆地上更加未知且多变的危险(Wang K et al.,Cell, 2021)。骨骼分泌的骨钙素(OCN)已被证明在能量代谢、糖脂稳态等方面具有重要作用,但其能否作为急性应激信号、通过特定脑区、细胞、特定分子调控机制,连接骨骼与大脑、代谢与行为,在危急时刻启动逃跑反应,还是未解之谜。
研究发现,Looming反应可显著提升血液OCN水平;老年鼠OCN下调伴随应激反应敏感性降低,OCN敲除小鼠得到类似结果,证实OCN参与该反应。VTA脑区补充OCN实验表明VTA是OCN发挥作用的关键脑区(图1)。在OCN受体研究中,通过敲除模型证明GPR37介导逃跑反应,且VTA的GABA能与谷氨酸能神经元上的GPR37起主要作用(图1)。电生理实验显示OCN通过调控VTA神经元钾电流影响神经元活性。单细胞测序与机器学习分析表明GPR37与钾通道THIK1、GPR158与GIRK1分别相关;π-FISH技术进一步证实GPR37与THIK1共表达于Type I神经元,GPR158与GIRK1共表达于Type II神经元(图2)。功能上,OCN通过GPR37抑制THIK1电流增强兴奋性,通过GPR158增强GIRK1电流导致抑制。机制上,GPR37通过非经典Gi通路降低cAMP、抑制THIK1通道,从而提升神经元兴奋性。行为学实验验证,VTA区阻断cAMP或特异性敲除THIK1通道均会削弱逃跑反应(图2)。
综上,本研究揭示了骨骼激素OCN在危急时刻启动本能逃跑反应的完整通路:OCN → 结合VTA GABA-Glu共释放的神经元上的GPR37 →降低cAMP→抑制THIK1钾通道→ 增强神经元兴奋性→ 触发快速逃跑行为。
该研究首次揭示了骨骼作为内分泌器官,通过分泌OCN调控中脑神经环路功能的全新机制,建立了“骨-脑轴”与生存行为调控的直接关联(图3)。这一发现不仅拓展了对跨器官协作调控神经行为的认知边界,更为骨质疏松共患抑郁、神经退行性疾病等跨系统疾病的治疗提供了新的干预靶点和视角。
beat365在线体育app脑认知与脑疾病研究所/深港脑科学创新研究院王立平研究员为本文最后通讯作者,刘雪梅副研究员、谭力铭研究员、李翔研究员为本文共同通讯作者,刘雪梅副研究员、博士后王帅毓、助理研究员赖娟为论文共同第一作者。该研究得到了四川大学华西医院蒋若天研究员、深圳先进院储军研究员的大力支持和帮助,研究也得到了深圳理工大学Helmut Kettenmann教授、韩明虎教授以及中国科技大学/先进院毕国强教授的指导。感谢科技创新2030“脑科学与类脑研究”重大项目、国自然重点项目、广东省卓越创新团队、广东省脑连接图谱重点实验室、深圳杰出人才项目、深圳神经精神调控工程重点实验室等基金对本研究的支持。感谢深圳市脑解析与脑模拟重大科技基础设施提供的设备与技术支持。

文章上线截图
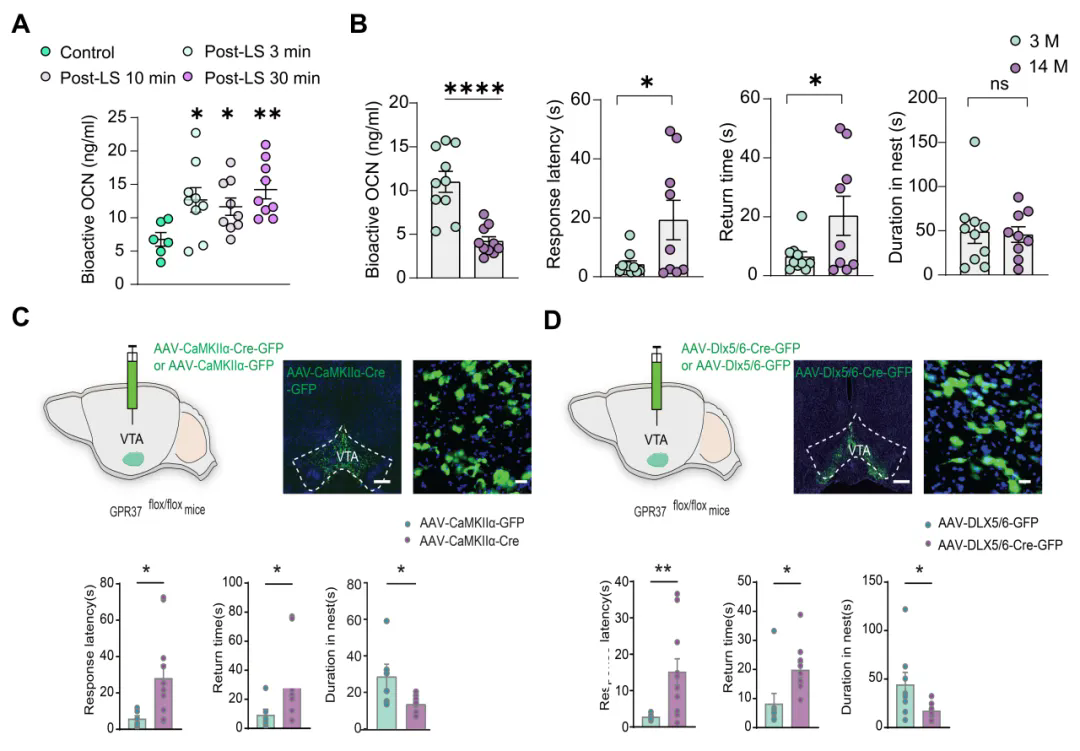
图1. OCN通过调控VTA脑区GABA能以及谷氨酸能神经元调控本能逃跑反应
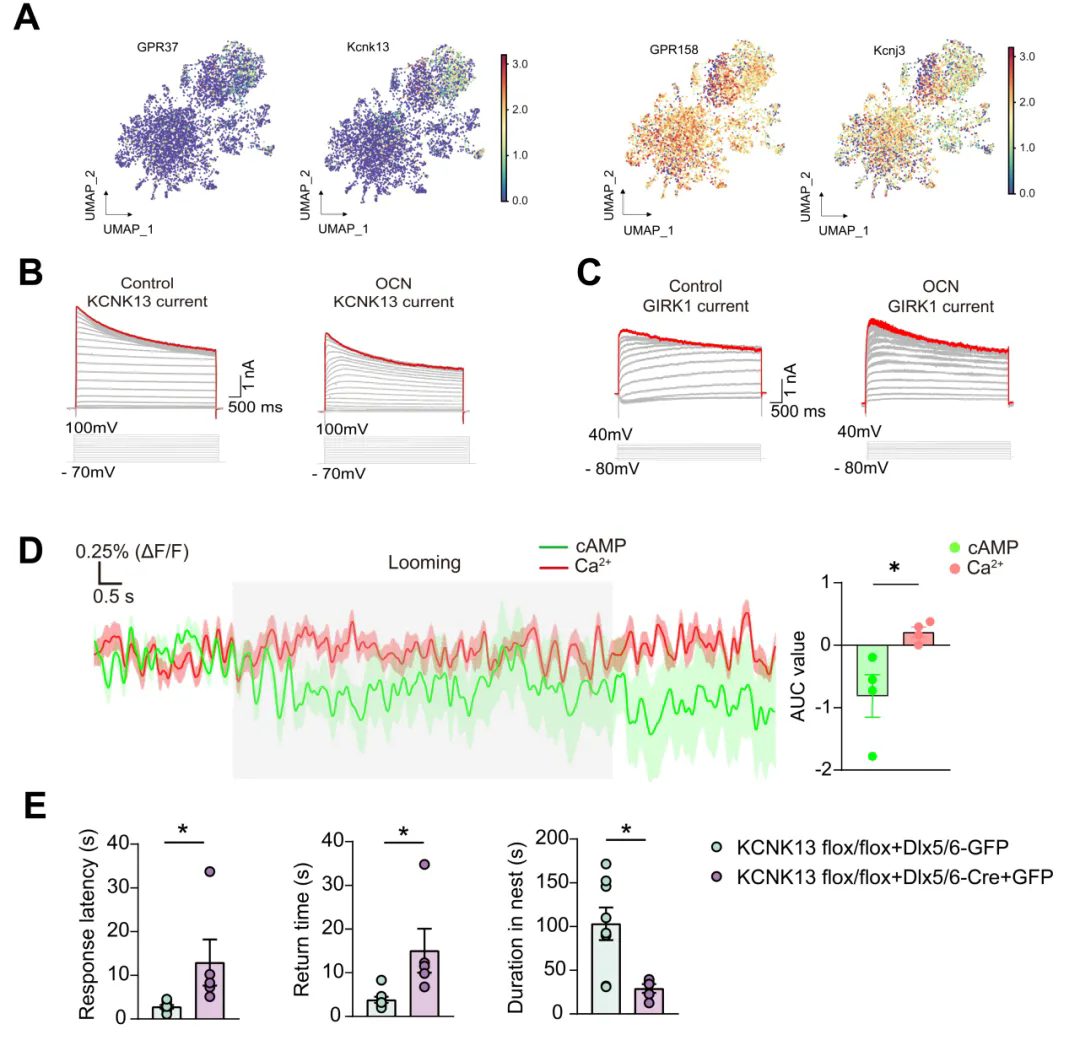
图2. OCN通过激活GPR37抑制cAMP水平和KCNK13通道介导本能逃跑反应
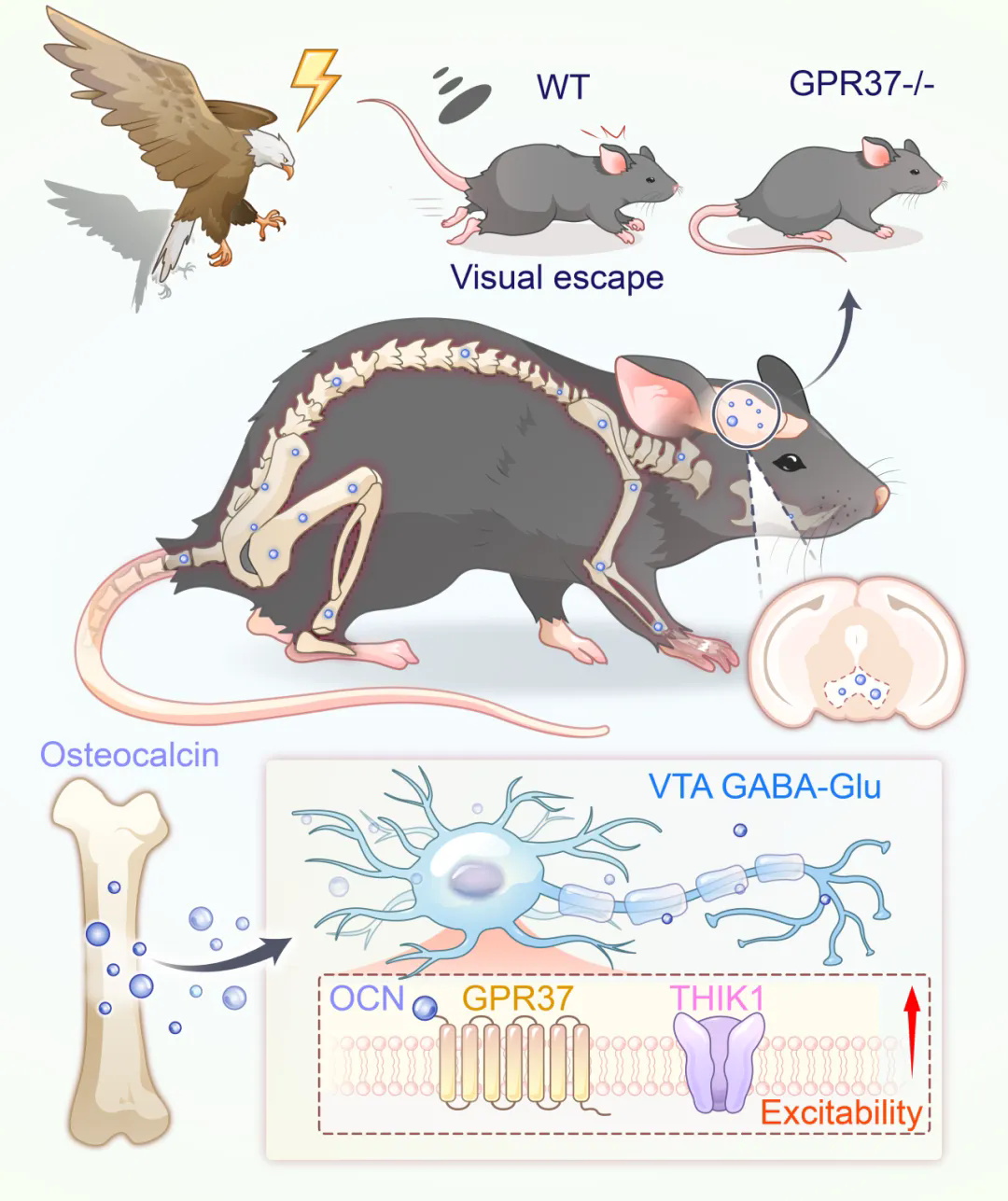
图3. “骨-脑轴”与生存行为调控研究示意图
附件下载: